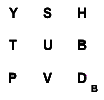Bimolekulare Reaktionen gleicher Teilchen
Für die Reaktion A + B → C ist die Herleitung der Geschwindigkeitsgleichung v = k x [A] x [B] über das Kollisionsmodell leicht möglich. Ausgehend von der Anzahl möglicher "produktiver" Kollisionen ([A] x [B]) wird durch Multiplikation mit k (Anteil der Kollisionen, die tatsächlich zur Reaktion führen) die Geschwindigkeit berechnet.
Problematischer ist die Betrachtung der Reaktion A + A → C. Prinzipiell ist der Ansatz v = k x "Kollisionsanzahl" immer sinnvoll möglich, es bleibt jedoch die Frage, wie man die Anzahl der Kollisionen berechnet. In den Lehrbüchern findet man eine Gleichung, die dem Ansatz der eingangs erläuterten Reaktion A + B → C entspricht: v = k x [A] x [A] oder v = k x [A]2. Dabei wird einfach das Teilchen B durch das Teilchen A ersetzt. Überprüft man dies an einfachen Beispielen, so stellt man jedoch fest, dass Unstimmigkeiten auftreten.
Aufgaben:
- Ermittle zur Wiederholung für die Reaktion A + B → C die Anzahl möglicher "produktiver" Kollisionen in einem System mit 3 Teilchen A und 3 Teilchen B. Verdeutliche dies anhand einer Skizze, in der die möglichen "produktiven" Kollisionen der einzelnen Teilchen untereinander eingezeichnet sind.
Vergleiche das Ergebnis der graphischen mit der über die Formel [A] x [B] berechneten Lösung. - Ermittle nun für die Reaktion A + A → C die Anzahl
möglicher "produktiver" Kollisionen in einem System mit 6 Teilchen A anhand einer Skizze, in der die
möglichen "produktiven" Kollisionen der einzelnen Teilchen
untereinander eingezeichnet sind.
Finde eine Formel zur Berechnung der über die graphische Lösung erhaltenen Anzahl von Kollisionen. Verallgemeinert ergibt sich die Formel n x (n-1) unter Verwendung von n für beliebige Teilchenzahlen. Vergleiche das Ergebnis mit dem in der Literatur zu findenden Ansatz [A] x [A] (also n x n) zur Berechnung. - Führe mit den beiden allgemeinen Gleichungen für die Reaktion A + A → C Berechnungen für Systeme mit 10, 100, 1000, 10.000, 100.000 .... bis 10 Mio Teilchen A durch. Vergleiche die mit den unterschiedlichen Formeln jeweils erhaltenen Werten unter Berechnung eines prozentualen Fehlers.
- Nimm Stellung zur Verwendung der Gleichung n x n in der Chemie (Stichwort "Mol").